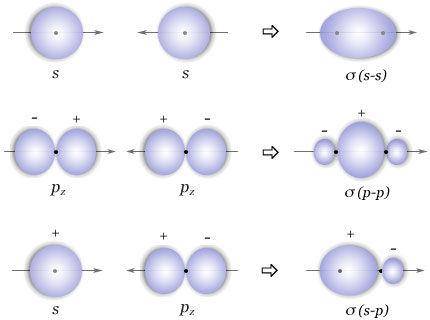
两个原子结合,是以共价键形式还是以离子键形式,主要取决于两个原子的电负性差值。电负性差值很大的金属和非金属结合,以离子键为主;电负性差值小的两个非金属结合,以共价键为主。共价键是电负性相同或相差不大的两个元素的原子相互作用时,原子之间通过共用电子对所形成的化学键。由共价键形成的化合物称为共价化合物。为了阐明这一类型的化学键问题,早在1916年,美国化学家路易斯(Lewis)就提出了原子间共用电子对的共价键理论。这一理论认为,分子中的每个原子力图通过共用一对或几对电子使其达到相应稀有气体原子的电子结构。
共价化合物与离子化合物之间最根本的区别在与是否存在离子键,因此可以通过熔融状态下是否产生电离来判断。在熔融条件下,共价键一般不会被破坏,可以认为共价化合物在熔融态下不电离。离子键一般能被破坏,所以离子化合物熔融状态下会发生电离,可以导电。特别地,属于共价化合物的盐(如AlCl₃, FeCl₃, (CH₃COO)₂Pb等)在熔融态视为不电离。
想要了解更多“共价化合物”的信息,请点击:共价化合物百科



